La Diabetis a l’edat pediàtrica
La diabetis mellitus tipus 1 (DM1) és la malaltia endocrinològica més freqüent a l’edat pediàtrica. Segons les dades del registre de la DM1 facilitades pel Consell Assessor de la diabetis, aproximadament el 50% de casos nous diagnosticats cada any a la nostra comunitat corresponen a pacients de 0 a 14 anys.
La freqüència de la malaltia és molt variable segons els diferents països i la seva presentació clínica (debut) té una estacionalitat clara en l’ edat pediàtrica, essent el diagnòstic més freqüent durant els mesos d’hivern, probablement relacionat amb la major incidència de quadres infecciosos intercurrents durant aquest mesos i que podrien actuar com a factor desencadenant del debut de la DM1.
Tot i que l’edat més freqüent de debut sempre s’ha situat al voltant del període d’inici de la pubertat, el cert és que cada vegada es diagnostiquen més pacients per sota dels 5 anys, i aquesta observació és similar a la del resta de països del nostre entorn. ( 1,2 )
Durant l’etapa infantil, no hi ha diferencies en quan a la distribució per sexes, però a partir de l’adolescència hi ha un increment del sexe masculí que és mantindrà durant els anys següents.
Actualment encara podem dir que, aproximadament el 95% dels casos diagnosticats de diabetis en l’edat pediàtrica, corresponen a diabetis tipus 1, però és possible que el percentatge d’altres tipus de diabetis pugui augmentar en els propers anys, principalment la diabetis tipus 2 que és troba en relació directe amb el important increment tant de la obesitat entre els nostres nens i adolescents.
Altres tipus de diabetis ja molt minoritàries serien aquelles secundàries a determinades malalties (fibrosi quística de pàncrees) o tractaments (corticoides, citostàtics....) que poden produir diabetis bé per insulinorresistència o per el seu efecte tòxic sobre les cèl•lules ß, la diabetis de origen genètic relacionada o no a defectes cromosòmics, com la diabetis tipus MODY s’ha de descartar davant d’un pacient diabètic nen o adolescent patró d’herència familiar autosòmica dominant. (3)
La diabetis neonatal és una entitat clínica diferent a la DM1, molt poc freqüent, que pot afectar a 1/400.000 nadons, i que sovint és relaciona també amb determinats defectes genètics. No té origen autoimmune, i en més de la meitat dels casos la diabetis pot ser transitòria desapareixent a les poques setmanes de vida.
2. Presentació clínica de la DM1 en l’edat pediàtrica
La presentació clínica pot ser molt variable depenent de l’edat del pacient. El període prodròmic en general és més curt que en etapes posteriors, principalment en els nens més petits.
Els símptomes inicials més freqüents és relacionen amb l’augment de la diüresis osmòtica (poliúria i nictúria) i la polidípsia. A diferència del que sol ocorre a l’adult, el augment de la gana (polifàgia) és poc freqüent en el nen donat l’aparició més precoç de cetosis que comporta anorèxia i pèrdua de pes.
Altres símptomes freqüents son l’abdominalgia i les infeccions cutànies recurrents, principalment les produïdes per fongs a l’àrea del bolquer en nens petits o en els genitals en edats posteriors (candidiasi)
En els adolescents la clínica inicial sol ser més similar a la del adult jove amb poliúria, nictúria i polidípsia, pèrdua de pes tot i la polifàgia; també poden mostrar-se astènics, referir visió borrosa i rampes a cames principalment per la nit o durant l’exercici.
La sospita diagnòstica en lactants pot ser difícil, la presentació clínica acostuma a ser aguda amb un quadre de deshidratació e irritabilitat en un nen en el que la poliúria dels dies previs ha pogut passa desapercebuda donat que porta bolquers. Els pares sovint no han notat símptomes suggestius durant els dies previs o de vegades refereixen una clínica de menys d’una setmana d’evolució.
En general, els nens d’edat menor presenten un debut clínic més agut, amb una major freqüència de cetoacidosi que és pot interpretar com una destrucció més ràpida de les cèl•lules ß. També es freqüent trobar nivells de pèptid c molt baixos i un període de remissió o “lluna de mel” més curt el que fa a pensar en la presencia d’un procés autoimmune més intens.
El diagnòstic de la diabetis en nens i adolescents acostuma a ser ràpid i fàcil. La hiperglucèmia deguda a altres patologies és molt infreqüent i en tot cas la presència de cetosis corrobora el diagnòstic de DM1.
La sospita diagnòstica ha de ser confirmada per les dades analítiques. Els criteris diagnòstics son els mateixos pels adults (ADA 1997, OMS 1998) que pels nens (ISPAD 2000) (4)
Les proves de laboratori, com el test de tolerància oral a la glucosa (TTOG) no acostumen a ser necessàries pel seu diagnòstic.
Els nivells de HbA1c solen estar més elevats en el moment del diagnòstic en el nens més grans que en els petits, donat que, com ja hem dit, aquets tenen una forma de presentació molt més ràpida i el període preclinic és més curt.
La presencia de marcadors d’autoimmunitat positius (anticossos antiGAD, anti insulina i IA2) confirmen l’origen autoimmune de la diabetis. La freqüència de presentació d’aquets anticossos en l’edat pediàtrica és variable:
antiGAD (80%), IA2 (70%) i antiinsulina (60%) però en nens menors de 5 anys la presencia d’aquest últims puja fins al 90%.
Al igual que en l’etapa adulta, el tractament amb insulina pretén també obtenir un bon control glucèmic però evitant al màxim les hipoglucèmies.(5)
El tractament insulínic és tindrà que anar adaptant durant les diferents etapes de desenvolupament del nen.
Els objectius glucèmics s’han d’establir en funció de l’edat del pacient i de la tendència o no a les hipoglucèmies freqüents.
De forma orientativa es poden establir el següents objectius glucèmics (mg/dl):
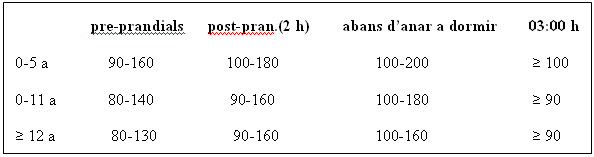
La pauta i dosi d’insulina en nens i adolescents s’ha d’establir de forma individualitzada. Els principals factors a tenir en comte son: edat, pes, desenvolupament puberal, temps d’evolució de la diabetis, alimentació i distribució horària, exercici físic i perfil glucèmic, valorant sobre tot la freqüència de hipoglucèmies.
Dosi d’insulina total (diària):

En alguns nens petits, amb necessitats d’insulina molt baixes, s’han d’utilitzar xeringues amb possibilitat de calcular mitges unitats (0,5 U) i /o insulines diluïdes de preparació en farmàcies hospitalàries.
En els nens i adolescents s’utilitzen les mateixes zones d’injecció que en els adults, però en lactants recomanen utilitzar més cuixes i natges, tot i que la zona del braç també està permesa sempre que els pares evitin la injecció intramuscular.
L’edat aconsellada per l’autoinjecció d’ insulina dependrà de cada nen però en general és convenient que comencin a partir dels 7-8 anys sempre amb la supervisió de un adult.
Com ja s’ha dit les pautes d’insulina s’han de anar modificant amb l’edat. La pauta bolus-basal amb la utilització dels anàlegs d’acció lenta (glargina o detemir) i ràpida (lispro o aspàrtica) son les més utilitzades actualment. Tot i això s’ha de tenir en compte que els nens i adolescents mengen més vegades que els adults donat que fan un segon esmorzar a l’escola i berenen, i el numero d’injeccions de anàlegs d’insulina ràpida pot ser entre 4 i 5 al dia..La proporció d’insulina basal en general és de un 40-50% del la dosi total diària.
En nens menors de 6 anys en els que la administració dels anàlegs d’insulina lenta no està encara aprovada, la insulinització es fa amb insulina NPH i insulina regular o anàlegs d’insulina ràpida abans dels àpats. La proporció d’insulina NPH és habitualment del 60-70% del total de la dosi diària.
Pautes d’insulina més utilitzades en l’edat pediàtrica:
Tot i el nombre d’injeccions d’insulina diàries, en general aquestes pautes son ben acceptades pels adolescents per la seva flexibilitat d’horaris i dieta.
La teràpia amb perfusor continu d’insulina subcutània (bombes d’insulina) ha presentat un increment important en els darrers anys en l’edat pediàtrica sobre tot en determinats països europeus i als Estats Units. (6)
El tractament amb bomba d’insulina subministra insulina de forma més fisiològica que el tractament amb dosi múltiples subcutànies obtenint una variabilitat glucèmica menor. Aquest tipus de tractament pot està indicat en aquells pacients que presenten un control glucèmic molt inestable o amb hipoglucèmies freqüents, principalment nocturnes. Això és especialment beneficiós en el nens més petits que presenten una major sensibilitat a la insulina i uns patrons de ingesta imprevisibles lo que els fa més vulnerables a les hipoglucèmies.
En altres grups d’edat com poden ser els adolescents, la teràpia amb bomba d’insulina pot ser la solució a problemes tan freqüents i de difícil solució com és el fenomen de l’ alba, donat que la bomba permet programar diferents patrons basals per cobrir les necessitats de cada pacient. (6,7)
L’alimentació del nen i adolescent amb diabetis ha de ser similar a la de qualsevol altre nen de la mateixa edat donat que els requeriments calòrics son iguals.
L’alimentació forma part del tractament de la diabetis i ha de ser variada, incloent tot tipus d’aliments i que permeti:
La dieta s’ha d’ intentar adaptar a cada pacient en funció dels seus hàbits dietètics, i de la seva família, dels horaris i de l’activitat física.
La composició de la dieta ha de incloure entre un 50-55 % d’hidrats de carboni del total de calories, un 30% de greixos (menor de 10% saturats) i entre un 15- 20% de proteïnes.
Per facilitar el control glucémic així com l’adaptació de la dieta a la pauta d’insulina, és fonamental que tant el pacient (a partir de certa edat) com la seva família calculin els hidrats de carboni segons el sistema de racions (1 ració = 10 gr d’hidrats) el que permet fer un correcte intercanvi i dona moltes més possibilitat a la dieta. (8)
Al igual que passa amb l’alimentació, la pràctica habitual d’exercici físic és molt aconsellable pel nen o adolescent amb diabetis com a part del seu tractament. A més dels beneficis comuns a la resta de nens, l’activitat física col•labora al bon control mantenint els nivells de glucosa i millorant la sensibilitat a la insulina. (9)
Amb una educació diabetològica adequada els nens i adolescents amb diabetis poden participar en tot tipus d’activitat física, controlant els nivells de glucosa abans, durant i desprès de la seva pràctica, i adequant la ingesta de hidrats de carboni i la pauta d’insulina al tipus d’activitat i la durada de la mateixa.
El diagnòstic de la diabetis en un nen o adolescent suposa un impacte psicològic dins de la família. L’adaptació a la malaltia és un procés dinàmic que passa per diferents fases d’acceptació. Les principals preocupacions que refereixen els pares son:
L’entorn sociocultural així com el grau d’estabilitat emocional de la família s’ha demostrat que poden influir en el control i evolució de la DM.
Al igual que en altres malalties cròniques, la diabetis en l’edat pediàtrica es pot associar amb alteracions psicològiques com problemes d’ansietat i d’adaptació a la malaltia. Els trastorns de la conducta alimentària (anorèxia i bulímia) son també més freqüents entre les adolescents amb diabetis que en la població general.(10)
Els problemes psicològics porten a una pitjor adherència al tractament i per tant a un control més deficient. La omissió de dosis d’insulina de forma voluntària o no s’ha de sospitar davant d’un adolescent amb mal control i episodis freqüents de cetoacidosi.
8. Complicacions de la DM1 a l’edat pediàtrica
Els resultats del Diabetes Control and Complications Trial (DCCT) (11) van demostrar la importància de mantenir un bon control glucèmic per evitar o endarrerir la aparició de les complicacions microvasculars de la DM1.
En el DCCT els resultats del tractament intensiu van ser pitjors dins del grup d’adolescents que en el grup dels adults amb valors de HbA1c mitja més elevats (8,1 vs 7,3 %). També es va objectivar un increment en el risc d’hipoglucèmies en part degudes als requeriments més elevats d’insulina en aquest grup d’edat secundària a la presència d’insulinorresistència.
També en aquest estudi es va evidenciar que els adolescents requereixen una major dedicació de temps i esforç per part dels equips diabetològics, son un grup de població més difícil de controlar i s’han de buscar alternatives terapèutiques que incrementin la seva collaboració.
En l’altre extrem de l’edat pediàtrica ens troben els nens petits (0-5 anys) que suposen reptes específics relacionats amb les diferències fisiològiques i de desenvolupament. Aquestes edats, a diferència de l’adolescència, es caracteritzen per una alta sensibilitat a la insulina, patrons d’ingesta irregulars, exercici molt variable, més vulnerabilitat a les hipoglucèmies amb menor capacitat per detectar-les i una possible més gran repercussió d’aquestes sobre les capacitats cognitives.
Tot i que fa uns anys és donava poca importància al control metabòlic dels anys previs a la pubertat, actualment se sap que la variabilitat glucèmica, la freqüència de les hipoglucèmies i els nivells de HbA1c elevats influeixen en la evolució posterior de la DM i en la aparició de les complicacions cròniques. (12)
El creixement i desenvolupament puberal és poden veure afectats quan el control metabòlic és molt deficient. En aquests casos és freqüent que el brot puberal es produeixi tard produint un efecte negatiu sobre el creixement.
Entenem per complicacions agudes de la DM1 els quadres de descompensació metabòlica aguda, es a dir la hipoglucèmia i la cetoacidosi.
La hipoglucèmia, que és defineix como la baixada del nivell de glucosa per sota de 60 mg/dl (3,3 mmol/L) és la complicació aguda més freqüent en el nen i adolescent. Acostuma a ser el resultat d’un desequilibri entre la dosi d’insulina administrada, la ingesta d’hidrats de carboni i la activitat física.
Tot i que en la major part dels casos els episodis son breus i autolimitats, acostuma a ser el problema que més angoixa als adolescents i als pares i això pot suposar un impediment per optimitzar el control glucèmic ajustant la dosis d’insulina. Sovint els pares dels nens més petits, s’excedeixen en el numero de controls de glucèmia per poder detectar-les.
Hi ha alguns estudis que parlen dels riscos de les hipoglucèmies repetides sobre el desenvolupament cerebral i cognitiu dels nens amb DM1. (13,14)
La clínica en el nen gran i adolescent és similar a la dels adults. En nens més petits, son els pares o cuidadors els que han de estar atents al símptomes suggestius com son la irritabilitat, sudoració, pallidesa o somnolència per poder tractar-la.
Es important que totes les persones que estan en contacte amb els nens amb diabetis (professors, monitors d’educació física, cangurs...) tinguin coneixement dels símptomes de la hipoglucèmia i de com és tracta. S’aconsella que els nens i adolescents portin algun tipus de identificació (placa, carnet...) on constin les seves dades i els diagnòstic de DM per tal de poder ajudar-los en cas de pèrdua de coneixement.
El tractament de la hipoglucèmia és la administració de sucre o altres hidrats d’absorció ràpida seguits de hidrats d’absorció lenta una vegada recuperat el nivell de glucèmia.
En els casos d’hipoglucèmia greu amb pèrdua de coneixement o convulsions, s’ha d’administrar el glucagó subcutani o intramuscular amb una dosi que variarà segons l’ edat i pes del pacient. En general es recomana 0,25 mg (1/4 de vial) en nens de menys de 10 kg, 0,50 mg (1/2 vial) de 10 a 25 kg i 1 mg (el vial sencer) per sobre d’aquest pes.
La cetoacidosi diabètica es produeix com a resultat de un dèficit absolut o relatiu d’insulina que condueix a greus alteracions metabòliques.(4,15,16) Es la causa més freqüent de hospitalització del nen diabètic. Ve definida per uns paràmetres bioquímics:
La cetoacidosi pot ser la forma de presentació inicial de la diabetis, tot i que cada vegada és menys freqüent gràcies al diagnòstic més precoç de la malaltia per part dels pediatres.
La complicació més greu és l’edema cerebral que es pot presentar entre un 0,3-1% dels casos, i és la principal causa de mortalitat en l’edat pediàtrica relacionada amb la diabetis.(17)
Els símptomes de la cetoacidosi son molt variables dependent de l’edat i de la gravetat del quadre clínic. En la major part dels casos es presenta com una deshidratació aguda amb poliúria, polidípsia, abdominalgia amb vòmits, respiració acidòtica, fetor cetonèmic i alteració del nivell de consciència.
El tractament de la cetoacidosi en el moment del debut sempre es durà a terme dins d’un centre hospitalari i per personal ben format.
En els pacients ja diagnosticats, si la cetoacidosi es lleu o moderada i la tolerància oral es bona, pot ser tractada de forma ambulatòria, inclús en el mateix domicili amb el suport del equip diabetològic.
El risc de poder patir complicacions cròniques relacionades amb el mal control de la diabetis és un tema que s’ha de parlar amb els adolescents i les seves famílies. La informació que es dona a l’adolescent ha de ser gradual i adequada a la seva edat.
Els anys corresponents a la pubertat poden accelerar la progressió de les complicacions microvasculars (retinopatia, nefropatia i neuropatia) (18,19)
Les complicacions microvasculars precoces son subclíniques però poden ser detectades aplicant els mètodes necessaris.
Els protocols de seguiment de l’ISPAD (International Society for Pediatric and Adolescent Diabetes) (4) aconsellen controlar la funció renal (detecció de la microalbuminúria) i el fons de l’ull anualment a partir del segon any d’evolució en tots els adolescents. Abans de la pubertat el control es farà cada cinc anys.
Es important el control de la tensió arterial sobre tot en els pacients amb antecedents familiars de hipertensió o nefropatia. La neuropatia clínica és molt poc freqüent en l’edat pediàtrica, però s’ha de fer un electromiograma als pacients que refereixin clínica de dolor o rampes a extremitats inferiors.
La aparició de complicacions macrovasculars és molt rara abans dels 30 anys, tot i així durant l’adolescència s`han de controlar els factors de risc que predisposen a aquestes complicacions com son la hipertensió arterial, la dislipèmia, el tabac, l’obesitat i la presencia de microalbuminuria y/neuropatia.
Per últim dir que la diabetis tipus 1 es pot associar a altres patologies com son:
1. Soltesz G. Diabetes in the young: a paediatric and epidemiological perspective. Diabetologia 2003; Apr; 46(4): 447-54
2. Green A, Patterson CC; EURODIAB TIGER STUDY GROUP. Trends in the incidence of childhood-onset diabetes in Europe 1989-1998. Diabetologia 2001; Oct; 44 Suppl 3: 33-8
3. Ize-Ludlow D, Sperling MK. The classification of diabetis Mellitus: A conceptual framework. Diabetes Mellitus in children. Pediatric Clinics of North America 2005; vol 52: 1533-52
4. International Society for Pediatric and Adolescent Diabetes: ISPAD Consensus Guidelines for the Management of Type 1 Diabetes Mellitus in children and adolescents. Zeist, Netherlands. Medforum, 2000
5. Silverstein J, Klingensmith G et al. Care of children and adolescent with type 1 diabetes: a statement of the American Diabets Association. Diabetes Care 2005 Jan; 28 (1): 186-212
6. Low KG, Massa L, Lehman D, et al. Insulina pump use in young adolescents with type 1 diabetes: a descriptive study. Pediatr Diabetes 2005; 6: 22-31
7. Battelino T. Risk and benefits of continuous subcutaneous insulin infusion (CSII) treatment in school children and adolescents. Pediatr Diabetes 2006 Aug, 7 Suppl 4: 25-31
8. Waldron S, Hanas R, Palming B. How do we educate young people to balance carbohydrate intake with adjustements of insulin?. Horm Res 2002; 57: 562-65
9. Riddell MC, Iscoe KE. Physical activity, sport, and pediatric diabetes. Pediatric Diabetes 2006; 7: 60-70
10. Moreland EC, Tovar A, Zuehlke JB, et al. The impact of physiological, therapeutic and psychosocial variables on glycemic control in youth with type one diabeties mellitus J Pediatr Endocrinol Metab 2004;17: 1533-44
11. The DCCT Research Group. The effect of intensive diabetes treatment on the development and progression of long-term complications in adolescents with insulin dependent diabetes mellitus. The Diabetes Control and Complications Trial. J Pediatr 1994; 125: 177-188
12. Donaghe KC, Fairchild JM, Craig ME, et all. Do all prepuberal years of diabetes duration contribute equally to diabetes complications? Diabetes Care 2003; 26: 1224-29
13. Davis EA, Keating B, Byrne GC, et al. Hipoglycemia: incidence and clinical predictors in a large population based sample of children and adolescents with IDDM. Diabetes Care 1997; 20: 22-25
14. Bolsera MK, Holman CD, Davis EA et al. The impact of a decade of changing treatment on rates of severe hypoglycemia in a population-based cohort of children with type 1 diabetes. Diabetes Care 2004 Oct; 27(10): 2293-8
15. Wofsdorf J, Glaser N, Sperling MA. American Diabetes Association. Diabetes Ketoacidosis in infants, children and adolescents: A consensus statements from the American Diabetes Association. Diabetes Care 2006 May, 29(5): 1150-9
16. Dunger D, Sperling M, Acerini C, et al. ESPE/LWPES consensus statement on diabetic ketoacidosis in children and adolescent. Arch Dis Child 2003; 89: 1884-94
17. Blanc N, Lucidarme N, Tubiana-Rufi N, Factors associated with childhood diabetes manifesting as ketoacidosis and its severity. Arch Pediatr 2003; 10: 320-25
18. Bognetti E, Calori G, Meshi F, et al. Prevalence and correlations of early microvascular complications in young type 1 diabetes patients: role of puberty. J Pediatr Endocrinol 1997; 10: 587-92
19. Danemon D, Early diabetes related complications in adolescents; risk factors and screening. Horm Res. 2005; 63 (2): 75-85